நூலாசிரியர்:
Randy Alexander
உருவாக்கிய தேதி:
2 ஏப்ரல் 2021
புதுப்பிப்பு தேதி:
1 ஜூலை 2024

உள்ளடக்கம்
ஒரு வேதியியல் சமன்பாடு என்பது ஒரு வேதியியல் எதிர்வினையின் குறியீட்டு பிரதிநிதித்துவம் ஆகும். உலைகள் இடது புறத்திலும், தயாரிப்பு வலது புறத்திலும் எழுதப்பட்டுள்ளன. ஒரு வேதியியல் எதிர்வினையில் எந்த அணுக்களும் பிறக்கவில்லை அல்லது இழக்கப்படுவதில்லை என்பதை வெகுஜனத்தைப் பாதுகாக்கும் விதி குறிக்கிறது, எனவே எதிர்வினைகளில் இருக்கும் அணுக்களின் எண்ணிக்கை எதிர்வினையில் இருக்கும் அணுக்களின் எண்ணிக்கையுடன் சமமாக இருக்க வேண்டும். தயாரிப்பு. இந்த டுடோரியலைத் தொடர்ந்து, நீங்கள் வேதியியல் சமன்பாடுகளை வெவ்வேறு வழிகளில் சமப்படுத்தலாம்.
படிகள்
2 இன் முறை 1: பாரம்பரிய முறைப்படி சமநிலை
கொடுக்கப்பட்ட சமன்பாட்டை எழுதுங்கள். இந்த எடுத்துக்காட்டில், உங்களிடம்: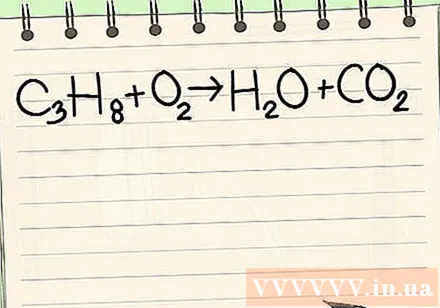
- சி3எச்8 + ஓ2 -> எச்2O + CO2
- புரோபேன் (சி3எச்8நீர் மற்றும் கார்பன் டை ஆக்சைடை உருவாக்க ஆக்ஸிஜனில் எரிக்கப்படுகிறது.

சமன்பாட்டின் ஒவ்வொரு பக்கத்திலும் உங்களிடம் உள்ள ஒவ்வொரு உறுப்புக்கும் அணுக்களின் எண்ணிக்கையை எழுதுங்கள். சமன்பாட்டில் உள்ள அணுக்களின் எண்ணிக்கையைக் கண்டறிய ஒவ்வொரு அணுவிற்கும் அடுத்துள்ள குறியீடுகளைக் காண்க.- இடது: 3 கார்பன், 8 ஹைட்ரஜன் மற்றும் 2 ஆக்ஸிஜன்.
- வலது: 1 கார்பன், 2 ஹைட்ரஜன் மற்றும் 3 ஆக்ஸிஜன்.
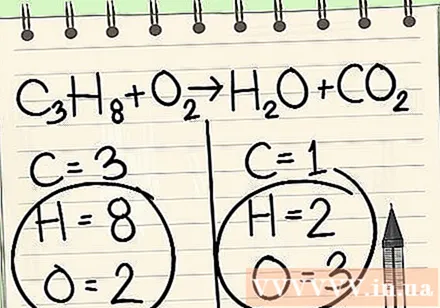
எப்போதும் ஹைட்ரஜன் மற்றும் ஆக்ஸிஜனை முடிவில் விட்டு விடுங்கள்.
சமநிலைப்படுத்த உங்களிடம் ஒன்றுக்கு மேற்பட்ட உறுப்பு இருந்தால்: எதிர்வினையின் ஒற்றை மூலக்கூறிலும், உற்பத்தியின் ஒற்றை மூலக்கூறிலும் மட்டுமே தோன்றும் ஒரு உறுப்பைத் தேர்ந்தெடுக்கவும். இதன் பொருள் நீங்கள் முதலில் கார்பன் அணுக்களை சமப்படுத்த வேண்டும்.
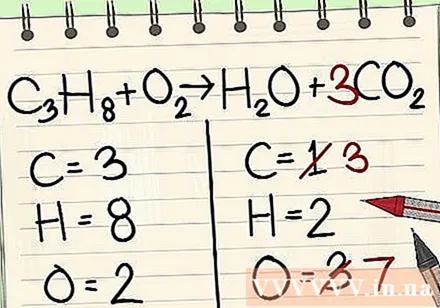
சமன்பாட்டின் இடது பக்கத்தில் உள்ள மூன்று கார்பன் அணுக்களுடன் சமப்படுத்த ஒற்றை கார்பன் அணுக்களுக்கான குணகத்தை சமன்பாட்டின் வலது பக்கத்தில் சேர்க்கவும்.- சி3எச்8 + ஓ2 -> எச்2O + 3CO2
- வலதுபுறத்தில் கார்பனுக்கு முன்னால் 3 இன் ஒரு காரணி 3 கார்பன் அணுக்கள் இருப்பதைக் குறிக்கிறது, இடது பக்கத்தில் 3 க்குக் கீழே உள்ள குறியீடு 3 கார்பன் அணுக்களைக் குறிக்கிறது.
- ஒரு வேதியியல் சமன்பாட்டில், நீங்கள் குணகத்தை மாற்றலாம், ஆனால் சந்தா அல்ல.
அடுத்தது ஹைட்ரஜன் அணு சமநிலை. உங்களிடம் இடதுபுறத்தில் 8 ஹைட்ரஜன் அணுக்கள் உள்ளன. எனவே உங்களுக்கு வலது பக்கத்தில் 8 தேவைப்படும்.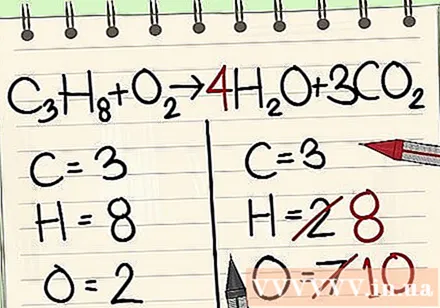
- சி3எச்8 + ஓ2 -> 4 எச்2O + 3CO2
- வலதுபுறத்தில் இப்போது 4 ஐ காரணியாகச் சேர்க்கவும், ஏனெனில் கீழே உள்ள எண் உங்களிடம் ஏற்கனவே 2 ஹைட்ரஜன் அணுக்கள் இருப்பதைக் காட்டுகிறது.
- நீங்கள் காரணி 4 ஐ குறியீட்டு 2 ஆல் பெருக்கும்போது, உங்களுக்கு 8 கிடைக்கும்.
- மற்ற 6 ஆக்ஸிஜன் அணுக்கள் 3CO இலிருந்து வந்தவை2. (3x2 = 6 ஆக்ஸிஜன் அணுக்கள் + 4 பிற ஆக்ஸிஜன் அணுக்கள் = 10)
ஆக்ஸிஜன் அணுக்களை சமநிலைப்படுத்துங்கள்.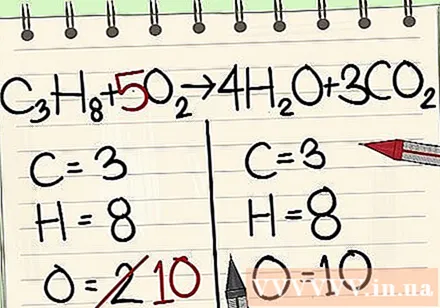
- சமன்பாட்டின் வலதுபுறத்தில் உள்ள மூலக்கூறுகளுக்கு நீங்கள் குணகங்களைச் சேர்த்துள்ளதால், ஆக்ஸிஜன் அணுக்களின் எண்ணிக்கை மாறிவிட்டது. இப்போது நீங்கள் நீர் மூலக்கூறில் 4 ஆக்ஸிஜன் அணுக்களும், கார்பன் டை ஆக்சைடு மூலக்கூறில் 6 ஆக்ஸிஜன் அணுக்களும் உள்ளன. மொத்தத்தில் நம்மிடம் 10 ஆக்ஸிஜன் அணுக்கள் உள்ளன.
- சமன்பாட்டின் இடதுபுறத்தில் ஆக்ஸிஜன் மூலக்கூறுக்கு 5 காரணி சேர்க்கவும். இப்போது நீங்கள் ஒவ்வொரு பக்கத்திலும் 10 ஆக்ஸிஜன் மூலக்கூறுகள் உள்ளன.
- சி3எச்8 + 5O2 -> 4 எச்2O + 3CO2.

- கார்பன், ஹைட்ரஜன் மற்றும் ஆக்ஸிஜன் அணுக்கள் சமநிலையில் உள்ளன. உங்கள் சமன்பாடு முடிந்தது.
முறை 2 இன் 2: இயற்கணித முறைப்படி சமநிலை
சின்னங்கள் மற்றும் சூத்திரங்களின்படி சமன்பாடுகளை எழுதுங்கள். ஒரு = 1 ஐ எடுத்துக்காட்டு மற்றும் அந்த சூத்திரத்தின் அடிப்படையில் சமன்பாட்டை எழுதவும்.
இலக்கங்களை அவற்றின் மாறிகள் மூலம் மாற்றவும்.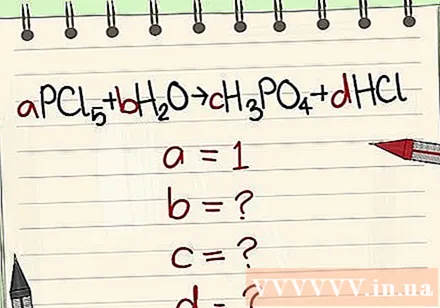
எதிர்வினை பக்கத்திலும், தயாரிப்பு பக்கத்திலும் உள்ள உறுப்புகளின் அளவை சரிபார்க்கவும்.
- எடுத்துக்காட்டு: aPCl5 + bH2O = cH3PO4 + dHCl இதனால் a = 1 b = c = d = மற்றும் P, Cl, H, O உறுப்புகளை பிரிக்கிறது, எனவே நீங்கள் ஒரு = 1 b = 4 c = 1 d = 5 .
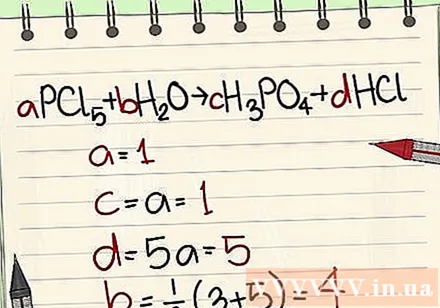
- எடுத்துக்காட்டு: aPCl5 + bH2O = cH3PO4 + dHCl இதனால் a = 1 b = c = d = மற்றும் P, Cl, H, O உறுப்புகளை பிரிக்கிறது, எனவே நீங்கள் ஒரு = 1 b = 4 c = 1 d = 5 .
ஆலோசனை
- சமன்பாட்டை எளிமைப்படுத்த நினைவில் கொள்ளுங்கள்.
- உங்களுக்கு சிக்கல் இருந்தால், அதை சமப்படுத்த ஆன்லைன் சமநிலை கருவியில் ஒரு சமன்பாட்டை தட்டச்சு செய்யலாம். நீங்கள் தேர்வுக்கு வரும்போது ஆன்லைன் இருப்புக்கான அணுகல் இல்லை என்பதை நினைவில் கொள்ளுங்கள், எனவே அதைச் சார்ந்து இருக்க வேண்டாம்.
எச்சரிக்கை
- ஒரு வேதியியல் சமன்பாட்டில் ஒருபோதும் ஒரு குணகத்தை ஒரு பகுதியாகப் பயன்படுத்த வேண்டாம் - நீங்கள் ஒரு வேதியியல் எதிர்வினையில் மூலக்கூறுகள் அல்லது அணுக்களைப் பிரிக்க முடியாது.
- சமநிலை செயல்பாட்டின் போது, நீங்கள் பின்னங்களைப் பயன்படுத்தலாம், ஆனால் குணகங்கள் இன்னும் பின்னங்களாக இருந்தால் சமன்பாடு சமப்படுத்தப்படாது.
- பின்னங்களை அகற்ற, முழு சமன்பாட்டையும் (இடது மற்றும் வலது இரண்டையும்) பின்னத்தின் வகுப்பால் பெருக்கவும்.



