நூலாசிரியர்:
Monica Porter
உருவாக்கிய தேதி:
17 மார்ச் 2021
புதுப்பிப்பு தேதி:
1 ஜூலை 2024

உள்ளடக்கம்
மோலார் செறிவு ஒரு கரைசலின் மோல்களின் எண்ணிக்கைக்கும் கரைசலின் அளவிற்கும் இடையிலான உறவைக் குறிக்கிறது. மோலாரிட்டியைக் கணக்கிட, நீங்கள் மோல் மற்றும் தொகுதி, நிறை மற்றும் அளவு அல்லது மோல் மற்றும் மில்லிலிட்டர்கள் (மில்லி) உடன் தொடங்கலாம். பின்னர், மேலே உள்ள மாறிகளுக்கு, சரியான முடிவைப் பெற அடிப்படை மோலார் செறிவு சூத்திரத்தைப் பயன்படுத்துங்கள்.
படிகள்
4 இன் முறை 1: மோலார் எண் மற்றும் தொகுதியிலிருந்து மோல் செறிவைக் கணக்கிடுங்கள்
மோலார் செறிவைக் கணக்கிடுவதற்கான அடிப்படை சூத்திரத்தை அறிந்து கொள்வது அவசியம். மோலார் செறிவு லிட்டர்களில் கரைசலின் அளவால் வகுக்கப்பட்ட ஒரு கரைசலின் மோல்களின் எண்ணிக்கைக்கு சமம். அங்கிருந்து, எங்களுக்கு பின்வரும் சூத்திரம் உள்ளது: மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் எண்ணிக்கை
- எடுத்துக்காட்டு: 4.2 லிட்டர் கரைசலில் NaCl இன் 0.75 மோல் கொண்ட ஒரு கரைசலின் மோலார் செறிவு என்ன?

தலைப்பை பகுப்பாய்வு செய்யுங்கள். மோலார் செறிவைக் கணக்கிட, உங்களுக்கு மோல்களின் எண்ணிக்கை மற்றும் லிட்டரில் கரைசலின் அளவு தேவை. கொடுக்கப்பட்ட தலைப்பின் காரணமாக இந்த இரண்டு மதிப்புகளையும் நீங்கள் கணக்கிட தேவையில்லை.- உதாரணத்திற்கு:
- மோல்களின் எண்ணிக்கை = NaCl இன் 0.75 மோல்
- தொகுதி = 4.2 எல்
- உதாரணத்திற்கு:
மோல்களின் எண்ணிக்கையை தொகுதி மூலம் வகுக்கவும். அளவின் அடிப்படையில் மோல் பிரிவின் விளைவாக ஒரு லிட்டர் கரைசலுக்கு மோல்களின் எண்ணிக்கை அல்லது அந்த கரைசலின் மோலார் செறிவு ஆகும்.
- எடுத்துக்காட்டு: மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் லிட்டர் எண்ணிக்கை = 0.75 மோல் / 4.2 எல் = 0.17857142

உங்கள் முடிவுகளை பதிவு செய்யுங்கள். ஆசிரியரின் கோரிக்கை அல்லது வேலையைப் பொறுத்து கமாவுக்குப் பிறகு இரண்டு அல்லது மூன்று எண்களைச் சுற்றவும். உங்கள் முடிவுகளைப் பதிவுசெய்யும்போது, "மோலார் செறிவு" ஐ "எம்" உடன் சுருக்கி, கரைசலின் ரசாயன சின்னத்தை சேர்க்கவும்.- உதாரணத்திற்கு: 0.179 எம் NaCl
4 இன் முறை 2: நிறை மற்றும் தொகுதியிலிருந்து மோல் செறிவைக் கணக்கிடுங்கள்
மோலார் செறிவைக் கணக்கிடுவதற்கான அடிப்படை சூத்திரத்தை அறிந்து கொள்வது அவசியம். மோலார் செறிவு ஒரு கரைசலின் மோல்களின் எண்ணிக்கைக்கும் கரைசலின் அளவிற்கும் இடையிலான உறவைக் காட்டுகிறது. மோலார் செறிவுக்கான சூத்திரம் பின்வருமாறு: மோலார் செறிவு = கரைப்பான் செறிவு / கரைசலின் எண்ணிக்கை
- சிக்கல் எடுத்துக்காட்டு: KMnO இன் 3.4 கிராம் கரைந்தவுடன் கரைசலின் மோல்களின் எண்ணிக்கையைக் கணக்கிடுங்கள்4 5.2 லிட்டர் தண்ணீரில்.

தலைப்பை பகுப்பாய்வு செய்யுங்கள்: மோலார் செறிவைக் கண்டுபிடிக்க, உங்களுக்கு மோல்களின் எண்ணிக்கை மற்றும் லிட்டரில் கரைசலின் அளவு தேவை. இந்த மதிப்புகள் வழங்கப்படாவிட்டால், ஆனால் தீர்வின் அளவு மற்றும் நிறை உங்களுக்குத் தெரிந்தால், மோலார் செறிவைக் கணக்கிடுவதற்கு முன் கரைப்பான் மோல்களின் எண்ணிக்கையை நீங்கள் தீர்மானிக்க முடியும்.- உதாரணத்திற்கு:
- எடை = 3.4 கிராம் KMnO4
- தொகுதி = 5.2 எல்
- உதாரணத்திற்கு:
கரைசலின் வெகுஜன மூலக்கூறைக் கணக்கிடுங்கள். அந்த வெகுஜனத்திலிருந்து அல்லது கிராம் கரைசலில் இருந்து கரைப்பான் மோல்களின் எண்ணிக்கையைக் கணக்கிட, நீங்கள் முதலில் கரைப்பான் வெகுஜன மூலக்கூறை தீர்மானிக்க வேண்டும். கரைசலில் ஒவ்வொரு தனிமத்தின் வெகுஜன அணுவையும் சேர்ப்பதன் மூலம் ஒரு கரைசலின் வெகுஜன மூலக்கூறு தீர்மானிக்க முடியும். ஒவ்வொரு தனிமத்தின் கன அணுவைக் கண்டுபிடிக்க, உறுப்புகளின் கால அட்டவணையைப் பயன்படுத்தவும்.
- உதாரணத்திற்கு:
- K = 39.1 கிராம் வெகுஜன அணு
- Mn = 54.9 கிராம் வெகுஜன அணு
- O = 16,0 கிராம் வெகுஜன அணு
- வெகுஜனத்தின் மொத்த அணுக்கள் = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 கிராம்
- உதாரணத்திற்கு:
கிராம் மோல்களாக மாற்றவும். நீங்கள் ஒரு கன மூலக்கூறு வைத்தவுடன், கரைசலில் ஒரு மோலார் வெகுஜனத்திற்கு 1 மோல் என்ற சமமான மாற்று காரணி மூலம் கரைசலில் கிராம் கரைசலின் எண்ணிக்கையை பெருக்க வேண்டும். இந்த பெருக்கத்தின் விளைவாக கரைப்பான் மோல்களின் எண்ணிக்கை.
- எடுத்துக்காட்டு: கிராம் கரைப்பான் * (1 / மோலார் வெகுஜன கரைசல்) = 3.4 கிராம் * (1 மோல் / 158 கிராம்) = 0.0215 மோல்
மோல்களின் எண்ணிக்கையை லிட்டர் எண்ணிக்கையால் வகுக்கவும். இப்போது நீங்கள் மோல்களின் எண்ணிக்கையை கணக்கிட்டுள்ளீர்கள், இப்போது அந்த எண்ணை கரைசலின் அளவைக் கொண்டு லிட்டரில் வகுக்கவும், அந்த கரைசலின் மோலார் செறிவு உங்களுக்கு இருக்கும்.
- எடுத்துக்காட்டு: மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் லிட்டர் எண்ணிக்கை = 0.0215 மோல் / 5.2 எல் = 0.004134615
உங்கள் முடிவுகளை பதிவு செய்யுங்கள். ஆசிரியருக்குத் தேவையான முடிவுகளை நீங்கள் சுற்றி வளைக்க வேண்டும், வழக்கமாக கமாவுக்குப் பிறகு இரண்டு முதல் மூன்று எண்கள். கூடுதலாக, முடிவை எழுதும் போது, "மோலார் செறிவு" ஐ "எம்" என்று சுருக்கி, கரைசலின் வேதியியல் சின்னத்துடன் செல்லுங்கள்.
- உதாரணத்திற்கு: 0.004 எம் KMnO4
4 இன் முறை 3: மோல் மற்றும் கரைசலின் மில்லிலிட்டர்களின் எண்ணிக்கையிலிருந்து மோலார் செறிவைக் கணக்கிடுங்கள்
மோலார் செறிவுக்கான சூத்திரத்தை அறிந்து கொள்ள வேண்டும். மோலார் செறிவைக் கணக்கிட. நீங்கள் ஒரு லிட்டர் கரைசலுக்கு கரைசலின் மோல்களின் எண்ணிக்கையை கணக்கிட வேண்டும், ஆனால் கரைசலின் மில்லிலிட்டர் அல்ல. மோலார் செறிவைக் கணக்கிடுவதற்கான பொதுவான சூத்திரம்: மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் எண்ணிக்கை
- எடுத்துக்காட்டு: CaCl இன் 1.2 மோல்களைக் கொண்ட ஒரு தீர்வின் மோலார் செறிவைக் கணக்கிடுங்கள்2 2905 மில்லிலிட்டர் தண்ணீரில்.
தலைப்பை பகுப்பாய்வு செய்யுங்கள். மோலார் செறிவைக் கணக்கிட, உங்களுக்கு கரைப்பான் மோல்களின் எண்ணிக்கையும் லிட்டரில் கரைசலின் அளவும் தேவை. மில்லிலிட்டர்களில் சிக்கலில் தீர்வின் அளவு கொடுக்கப்பட்டால், கணக்கீடு செய்வதற்கு முன் லிட்டரில் சமமான தொகுதிக்கு மாற்றவும்.
- உதாரணத்திற்கு:
- மோல்களின் எண்ணிக்கை = CaCl இன் 1.2 மோல்2
- தொகுதி = 2905 மிலி
- உதாரணத்திற்கு:
மில்லிலிட்டர்களை லிட்டராக மாற்றவும். கரைசலை மில்லிலிட்டரிலிருந்து லிட்டராக மாற்ற, மில்லிலிட்டர்களின் எண்ணிக்கையை 1000 ஆல் வகுக்கவும், ஏனெனில் ஒவ்வொரு லிட்டரும் 1000 மில்லிலிட்டர்களுக்கு சமம். எஞ்சியிருக்கும் தசம புள்ளியை மாற்றுவதன் மூலம் மில்லிலிட்டர்களை லிட்டராக மாற்றலாம்.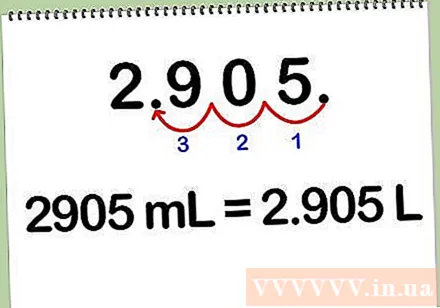
- உதாரணமாக: 2905 மிலி * (1 எல் / 1000 மில்லி) = 2,905 எல்
மோல்களின் எண்ணிக்கையை லிட்டர் எண்ணிக்கையால் வகுக்கவும். நீங்கள் லிட்டர் எண்ணிக்கையைப் பெற்ற பிறகு, மோலர்களின் எண்ணிக்கையை லிட்டர் கரைசலின் எண்ணிக்கையால் வகுப்பதன் மூலம் மோலார் செறிவைக் கணக்கிடலாம்.
- எடுத்துக்காட்டு: மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் லிட்டர் எண்ணிக்கை = CaCl இன் 1.2 மோல்2 / 2,905 எல் = 0.413080895
உங்கள் முடிவுகளை பதிவு செய்யுங்கள். முடிவை இரண்டு அல்லது மூன்று காற்புள்ளிகளுக்கு அல்லது உங்கள் ஆசிரியரின் வேண்டுகோளுக்கு இணங்க நினைவில் கொள்ளுங்கள். முடிவைப் பதிவுசெய்யும்போது, "மோலார் செறிவு" ஐ "எம்" என்றும், பின்னர் கரைப்பான் வேதியியல் சின்னம் என்றும் சுருக்கவும்.
- உதாரணத்திற்கு: 0.413 M CaCl2
4 இன் முறை 4: கூடுதல் பயிற்சி
5.2 கிராம் NaCl 800 மில்லி தண்ணீரில் கரைக்கும்போது ஒரு கரைசலின் மோலார் செறிவைக் கணக்கிடுங்கள். சிக்கலால் கொடுக்கப்பட்ட மதிப்புகளைத் தீர்மானித்தல்: கிராம் வெகுஜன மற்றும் மில்லிலிட்டர்களில் அளவு.
- நிறை = 5.2 கிராம் NaCl
- தொகுதி = 800 மில்லி தண்ணீர்
Na தனிமத்தின் கன அணுவையும், Cl இன் கன அணுவையும் சேர்ப்பதன் மூலம் NaCl இன் வெகுஜன மூலக்கூறைக் கண்டறியவும்.
- Na = 22.99 கிராம் வெகுஜன அணு
- Cl = 35.45 கிராம் வெகுஜன அணு
- NaCl = 22.99 + 35.45 = 58.44 கிராம் வெகுஜன மூலக்கூறுகள்
மோலார் மாற்று காரணி மூலம் கரைப்பான் வெகுஜனத்தை பெருக்கவும். இந்த எடுத்துக்காட்டில், NaCl இன் மூலக்கூறு நிறை 58.44 கிராம், எனவே மாற்று காரணி “1 mol / 58.44 g” ஆகும்.
- NaCl மோலின் எண்ணிக்கை = 5.2 கிராம் NaCl * (1 mol / 58.44 g) = 0.8898 mol = 0.09 mol
800 மில்லி தண்ணீரை 1000 ஆல் வகுத்தால், நீங்கள் லிட்டரில் நீரின் அளவைப் பெறுவீர்கள்.
- மில்லிலிட்டரிலிருந்து லிட்டருக்கு 1 எல் / 1000 மில்லி மாற்றும் காரணியால் 800 மில்லி பெருக்கலாம்.
- மேலே உள்ள பெருக்கல் செயல்முறையை சுருக்க, நீங்கள் தசம புள்ளி 3 இலக்கங்களை இடதுபுறமாக ஆதரிக்கலாம்.
- தொகுதி = 800 மில்லி * (1 எல் / 1000 மில்லி) = 800 மில்லி / 1000 மில்லி = 0.8 எல்
கரைசலின் மோல்களின் எண்ணிக்கையை லிட்டரில் கரைசலின் அளவால் வகுக்கவும். மோலார் செறிவைக் கணக்கிட, நீங்கள் 0.09 மோல் கரைசலை (இந்த விஷயத்தில், NaCl) லிட்டரில் கரைசலின் அளவு மூலம் பிரிக்க வேண்டும்.
- மோலார் செறிவு = கரைப்பான் மோல்களின் எண்ணிக்கை / கரைசலின் எண்ணிக்கை = 0.09 மோல் / 0.8 எல் = 0.1125 மோல் / எல்
இறுதி முடிவை பதிவு செய்யுங்கள். கமாவுக்குப் பிறகு முடிவை இரண்டு அல்லது மூன்று இலக்கங்களாக வட்டமிட்டு, "மோலார் செறிவு" ஐ "எம்" உடன் சுருக்கமாக இரசாயன இரசாயன சின்னத்துடன் சுருக்கவும்.
- விளைவாக: 0.11 எம் NaCl